
29 mei 2019
Depressie en Parkinson
Een veel voorkomend duo in de spotlight
Het is ontzettend belangrijk dat neurologen zich realiseren dat depressie en cognitieve problemen bij Parkinson een groot ding is. Heel veel neurologen zijn hier nog onvoldoende van op de hoogte. Sterker nog, sommige neurologen zeggen: “Dit soort dingen is niks voor mij”. Maar het hoort er toch echt bij | Monique Timmer
Op 16 april 2019 promoveerde Monique Timmer op het proefschrift met de titel: “Out of Balance. Neurocognitive mechanisms underlying depression in Parkinson’s disease” (1). Benieuwd als ik ben naar de oorzaken en impact van neuropsychologische symptomen van de ziekte van Parkinson, stelde ik Monique 11 vragen om haar onderzoeksresultaten toe te lichten.
De ziekte van Parkinson kenmerkt zich door een massaal verlies van dopamine-producerende neuronen in een kleine kern in de hersenstam, de substantia nigra (2).
Dopamine is een neurotransmitter, een signaalstof die impulsen overdraagt van zenuwcel naar zenuwcel. Met deze signalen stuurt ons brein onze bewegingen aan. Bewegingen die variëren van lopen, praten, lachen en schrijven tot bijvoorbeeld de samentrekking van maag- en darmspieren. Naarmate de degeneratie van de substantia nigra vordert, wordt het steeds lastiger bewegingen aan te sturen. Dat leidt tot allerhande motorische symptomen, zoals traagheid van bewegen, stijfheid en tremor.

Maar dat is niet het hele verhaal. De neurodegeneratie in patiënten met de ziekte van Parkinson beperkt zich niet tot de substantia nigra. Ook andere hersengebieden worden in meer of mindere mate aangetast en deze aantasting draagt, naast de aantasting van het dopaminerge systeem, bij aan het ontstaan van zogenaamde niet-motorische symptomen, zoals bijvoorbeeld slaapproblemen en vele neuropsychologische symptomen zoals problemen in het denken, angststoornissen, apathie en depressie. Depressie is een van de meest voorkomende niet-motorische symptomen bij Parkinson.
Bij patiënten met depressie zijn bijvoorbeeld ook de loecus coerulus en de raphne nuclei aantoonbaar aangetast. In de locus coerulus huisvesten zich noradrenaline producerende neuronen en in de raphe nuclei serotonine producerende neuronen.

Depressie bij patiënten met de ziekte van Parkinson komt vaak voor. De schattingen lopen uiteen, maar gemiddeld 35% van de patiënten lijdt aan een klinisch relevante depressie. Toch wordt een depressie vaak niet als dusdanig herkend. Dat komt enerzijds omdat een deel van de symptomen ook bij Parkinsonpatiënten zonder depressie voorkomt. Denk bijvoorbeeld aan het afvlakken van de gelaatsuitdrukking, langzaam bewegen en zachter praten, slaapstoornissen, een gebrek aan energie en een verminderd vermogen ergens de aandacht bij te houden. Als we daar nog bij op tellen dat patiënten er zelf er ook niet zo makkelijk voor uit komen dat ze depressieve klachten ervaren, dan is het duidelijk dat depressie vaak over het hoofd wordt gezien.
Om de diagnose depressie bij mensen met de ziekte van Parkinson te stellen, is het zaak om achter het masker van de uiterlijke symptomen te kijken.

Dopaminerge betekent “gerelateerd aan dopamine”. Dopaminerge medicatie verhoogt de dopamine-gerelateerde activiteit in de hersenen. De meest voorgeschreven dopaminerge medicijnen zijn levodopa, een voorloperstof van dopamine en de zogeheten dopamine agonisten. Deze stoffen passen op de dopaminereceptor, zijn in staat deze te stimuleren en bootsen daarmee de werking van dopamine na. Bekende dopamine agonisten zijn ropinirol, pramipexol, rotigotine en apomorfine.

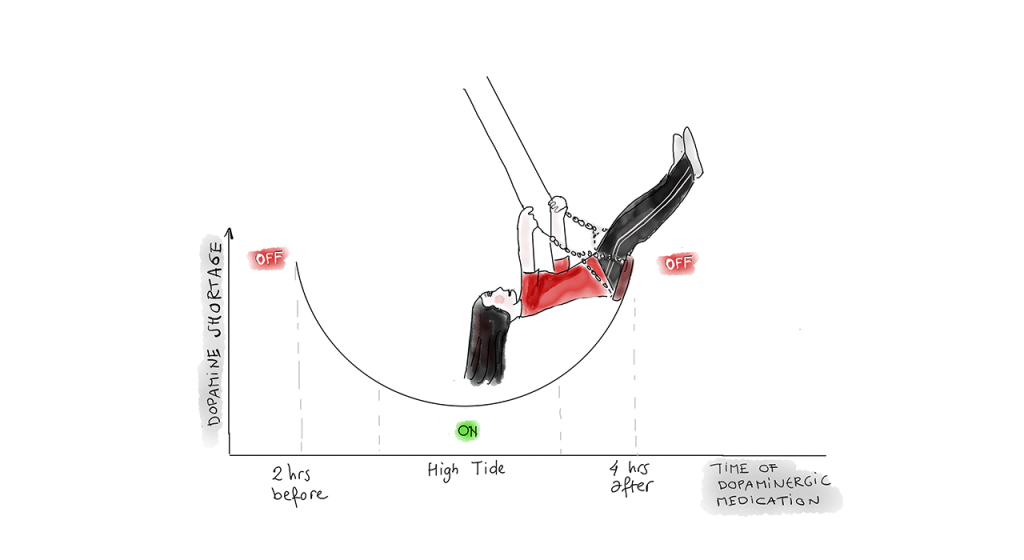
Een deel van de oorzaak van depressieve symptomen ligt in veranderingen in het dopaminerge systeem. Dat weten we, omdat een deel van de patiënten al voor het stellen van de diagnose ziekte van Parkinson een depressie of burn-out ervaart. Ook wordt hun vaak stemming beter zodra zij starten met dopaminerge medicatie. Daarnaast ervaart 75% van de patiënten niet alleen responsfluctuaties van de medicatie op hun motorische symptomen, maar ontstaan ook zogeheten mood swings (niet-motorische fluctuaties). Als de medicatie uitgewerkt raakt, en patiënten zijn OFF, dan zijn niet alleen hun motorische maar ook hun depressieve klachten ernstiger.
Maar de ene depressie is de andere niet. Bij sommige patiënten is de rol van het dopaminerge systeem groter dan bij andere. We weten nog niet waarom dat zo is. Daarnaast spelen ook andere neurotransmitter systemen, zoals het noradrenerge en serotonerge systeem, een belangrijke rol bij depressie. Wat deze rol precies is en hoe deze elkaar beïnvloeden bij depressie bij de ziekte van Parkinson is nog niet opgehelderd.
In het dagelijkse leven passen wij ons gedrag aan op basis van onze ervaringen. Patiënten met de ziekte van Parkinson en een vroegere of huidige depressie blijken minder goed te zijn in het leren van positieve ervaringen, terwijl zij net zo goed zijn in het leren van negatieve ervaringen als patiënten zonder depressieve klachten.
Ik zal een voorbeeld geven uit de praktijk: Stel, je hebt slechte ervaringen met een Sushi restaurant. Als een collega voorstelt om naar dat restaurant te gaan, ga je toch mee en tot je grote verrassing is het heel lekker. Je krijgt een onverwachte beloning en stelt je associatie bij. Als je de volgende keer weer besluit te gaan, ga je met hooggespannen verwachtingen. Dit keer blijkt het eten echter weer heel smerig te zijn. De vorige keer bleek er een inval kok aan het werk te zijn geweest en die is nu weer vertrokken. Je krijgt een onverwachte negatieve ervaring en stelt je associatie weer bij.
Parkinsonpatiënten met depressieve klachten zijn slechter in het omkeren van de associatie van een negatieve associatie naar een positieve associatie. Als we het voorbeeld van het Sushi restaurant weer aanhalen, dan zou dit bijvoorbeeld kunnen betekenen dat de patiënt in kwestie zijn associatie met het Sushi restaurant niet bijstelt op het moment dat het eten lekkerder blijkt dan verwacht. De volgende keer zou deze het restaurant alsnog overslaan.
Dit is slechts een voorbeeld om het principe te illustreren. Hoe groot het effect is, verschilt per patiënt. Mijn onderzoeksresultaten geven slechts aan dat er een relatie is tussen depressie en een verminderd vermogen om van een beloning te leren. Dit gedrag zien we overigens ook bij mensen met depressie zónder Parkinson.

Dopaminerge medicatie kan cognitieve functies verbeteren en verslechteren. Op het moment dat je dopaminerge medicatie krijgt, vult de hoeveelheid dopamine in een hersengebied dat het dorsale striatum heet weer aan. Dat maakt dat je weer beter kunt bewegen. Daarnaast verbeteren de cognitieve functies die met dit hersengebied geassocieerd worden, zoals het kunnen verleggen van je aandacht. Maar de medicatie komt ook in andere hersengebieden terecht. Als de dopamine terecht komt in hersengebieden die helemaal geen tekort aan dopamine hebben, dan kan dat juist leiden tot een overdosis, met het verslechteren van bepaalde cognitieve functies tot gevolg.
In mijn onderzoek heb ik – met de CANTAB-IED test – gekeken naar het vermogen van patiënten om hun associaties om te keren. Wat eerst goed was, veranderde in fout en vice versa. Dit cognitieve vermogen wordt in verband gebracht met een hersengebied dat het ventrale striatum heet. Bij patiënten met depressie, wordt gedacht dat dit gebied een tekort aan dopamine heeft. Bij patiënten zonder depressie niet.

Ik nam waar dat patiënten die meer dopaminerge medicatie slikten, slechter waren in het omkeren van dit soort associaties. Dat komt overeen met de overdosis theorie, waarbij het hersengebied met nog voldoende dopamine “overstroomt”, met verschillende negatieve cognitieve effecten tot gevolg. Maar, Parkinsonpatiënten mét een depressie bleken het allerslechtst te scoren. Dit resultaat hadden we niet verwacht, aangezien het betreffende hersengebied bij deze patiënten juist wordt geassocieerd met een tekort aan dopamine. Er spelen blijkbaar ook andere mechanismen een rol, zoals bijvoorbeeld het goed in balans kunnen houden van de dopamine spiegel zelf en ook de balans tussen dopamine en andere neurotransmitter systemen, zoals bijvoorbeeld het serotonerge systeem.
Maar ook al zijn de onderliggende mechanismen nog onbekend, toch is het een belangrijke ontdekking voor de behandelkamer. Neurologen zouden op basis van deze uitkomsten extra alert moeten zijn op de cognitieve bijwerkingen van dopaminerge medicatie en dan juist bij Parkinsonpatiënten mét een depressie.
We onderwierpen patiënten aan een gokspel, speciaal ontworpen om hun afkeer van verlies te meten. De deelnemers konden bij ieder gok, als het ware kop of munt, steeds tussen de 6 euro en 30 euro winnen en tussen de 3 en 15 euro verliezen. Deze set-up is gebaseerd op de aanname dat mensen gemiddeld genomen twee keer zo gevoelig zijn voor verlies dan voor winst. We testten patiënten zonder en met depressie twee keer. Een keer als ze ON waren, na inname van medicatie, en een keer nadat ze minstens 18 uur geen medicatie hadden ingenomen.
Patiënten zonder depressie gingen zonder medicatie überhaupt minder de gok aan. De hoogte van de bedragen maakte daarbij niet uit. Patiënten mét depressie gokten zonder medicatie ook minder, maar dat was juist omdat zij relatief gevoeliger voor verlies waren. Het winstbedrag moest relatief hoger zijn, wilden ze de gok aangaan. Patiënten zonder en met depressie lijken dus beiden, zonder medicatie, meer risicomijdend, maar via andere mechanismen. Ik zeg lijken, omdat we dit niet formeel met gezonde proefpersonen hebben kunnen vergelijken.

Na het slikken van dopaminerge medicatie normaliseerde het gedrag van beide groepen Parkinsonpatiënten. De medicatie verandert dus de beslissing van Parkinsonpatiënten om wel of niet een gok te wagen. Parkinsonpatiënten zonder depressieve klachten accepteerden vaker een gok, ongeacht het bedrag van de gok, terwijl depressieve patiënten vaker een gok accepteerden, omdat de medicatie ervoor zorgde dat ze minder verlies avers werden.
We deden met onze proefpersonen een zogeheten Stroop test. De proefpersonen krijgen dan bijvoorbeeld een pijl te zien die naar rechts wijst met het woord ‘LINKS’ erin en andersom. De ene keer werd hen gevraagd op de pijl te reageren, de andere keer op het woord in de pijl. De helft van de tests werden voorafgegaan door een beloning van 10 cent en de andere helft door een beloning van 1 cent.
Parkinsonpatiënten bleken hun aandacht gemakkelijker te kunnen wisselen van de richting van de pijl naar het woord in de pijl en vice versa als de beloning hoger was. Dat was zowel het geval bij patiënten met als zonder depressie.. Dit in tegenstelling tot gezonde proefpersonen, die maakten juist meer fouten bij een hogere beloning. Al met al kunnen we concluderen dat patiënten met Parkinson baat lijken te hebben bij een beloning als motivator om het wisselen van de aandacht tussen verschillende taken te stimuleren.

Voor mij heeft mijn promotieonderzoek heel erg geholpen om aan patiënten uit te leggen wat er in hun hersenen gebeurt bij depressieve symptomen en cognitieve klachten. En dat helpt patiënten om deze symptomen makkelijker te accepteren en aan de omgeving uit te leggen. Het is best een klus om om te gaan met een ziekte die meer beren op de weg zet en waarin je tegelijkertijd minder gemotiveerd bent om de beren uit de weg te ruimen. Deze ziekte vraagt dan ook juist om een hele positieve manier van benaderen. Als je zichtbaar en inzichtelijk kunt maken wat er aan de hand is en waarom dat gebeurt, wordt het minder beladen en dat kan helpen om conflicten – bijvoorbeeld tussen partners – te voorkomen.
Wellicht kun je patiënten een beloning voorschotelen. Bijvoorbeeld: “We gaan wandelen naar het park en daar gaan we een ijsje eten”. Maar uiteindelijk is iedere patiënt en partner – en dus iedere relatie – anders en moet ieder daar zijn/haar eigen weg in vinden. Maar het helpt enorm als je af en toe samen kunt uitzoomen om te kijken wat er gebeurt. En om vervolgens uit te proberen wat er wel en niet werkt.

Het is ontzettend belangrijk dat neurologen zich realiseren dat depressie en cognitieve problemen bij Parkinson een groot ding is. Heel veel neurologen zijn hier nog onvoldoende van op de hoogte. Sterker nog, sommige neurologen zeggen: “Dit soort dingen is niks voor mij”. Maar het hoort er toch echt bij.
Ik heb met mijn proefschrift aangetoond dat we waakzaam moeten zijn voor de negatieve effecten van dopaminerge medicatie op de cognitie, juist bij patiënten met depressie. Hoe eerder je dit soort effecten signaleert, hoe eerder je bij kunt sturen.
Gelukkig wordt er steeds meer onderzoek naar gedaan, maar er is nog wel een weg te gaan. In de tussentijd draag ik mijn steentje bij aan bewustwording met presentaties in de regio, poster presentaties op congressen en het wetenschappelijke artikel: “What a neurologist should know about depression in Parkinson’s disease” (3).
Waarom is het werk van Monique belangrijk voor mij?
Het onderzoek van Monique Timmer biedt prachtige aanknopingspunten voor een goede discussie over de impact van neuropsychologische symptomen bij de ziekte van Parkinson. Pas als je zichtbaar maakt wat er aan de hand is, kun je er mee omgaan of er zelfs een weg omheen vinden.
Het landschap der omweggetjes bij motorische freezing wordt al volop gedocumenteerd en nieuwe vindingen blijven het nieuws binnenstromen. Van de week was de trillende sok bijvoorbeeld het onderwerp van getril op mijn app. Er bestaan zeker ook algemene aanwijzingen voor het behoud van de cognitieve gezondheid bij Parkinson (4), maar een concreet overzicht van strategiëen en omweggetjes bij diverse typen van mentale freezing heb ik nog niet onder ogen gekregen. Mentale freezing is diffuser, minder concreet, minder bespreekbaar, minder onderzocht, minder zichtbaar en ook simpelweg minder sexy dan motorische freezing. Dat is onterecht, want de impact van mentale freezing op de levenskwaliteit is enorm. Je kunt er tenslotte van verdwijnen als mens.
Als ik iets tot mijn persoonlijke missie heb gemaakt, is het wel dat ik omweggetjes bij neuropsychologische symptomen wil verzamelen en aansluitend ook hoop om te toveren tot concrete hulpmiddelen voor patiënten en hun naasten. Het is soms ontzettend eenzaam in het land van Parkinson en het is echt fijn als er een aantal mensen mee kan reizen om – al verdwalend – samen het nieuwe landschap in te kleuren.
Om een omweggetjesbeginnetje te maken, doe ik hierbij alvast een drietal ervaringsduiten in het zakje:
Als ik cognitieve startproblemen heb, kun je proberen mij weer op gang te brengen door vragen, opdrachten en voorstellen op te knippen in onderdelen en zo concreet mogelijk – in hapklare brokken – voor te schotelen, bijvoorbeeld door:
- Een concrete vraag te stellen
Vraag niet ‘Hoe gaat het?’ Ik heb namelijk werkelijk geen idee waar ik dan moet starten.
Vraag liever naar iets specifieks zoals bijvoorbeeld: ’Hoe gaat het met de studie van je zoon?” - Alle stappen te benoemen
Stel midden in het bos – waar geen koffietent is – niet voor om samen koffie te drinken want het kan zijn dat ik dan niet reageer. Mijn gebrek aan reactie kan onaardig overkomen, maar is niet zo bedoeld. Feitelijk ben ik heel hard aan het zoeken naar een beginnetje. Er zijn namelijk zoveel wegen in mijn hersenen die naar koffie kunnen leiden dat ik niet zou weten waar ik moet starten.
Wat je kunt doen als je een reactie wilt, is het benoemen van de de stappen die je voor je ziet. Bijvoorbeeld: ‘Zullen we naar de auto lopen, naar jouw huis rijden en dan nog een kopje koffie drinken?’ Reken maar dat ik dan een antwoord geef.
Kijk niet alleen naar de inhoud van een gesprek maar ook naar het proces. Zoom geregeld even uit, observeer hoe het gesprek loopt en nodig me actief uit om mijn gedachten te delen. Een vriendin van mij vraagt soms: ‘Ben je nog aangehaakt?’ Mocht ik op dat moment toch niet meer uitgebreid kunnen antwoorden omdat mijn medicatiespiegel te laag is geworden, dan kan jij of ik er ook later op terug komen.
Soms willen de woorden niet komen. Dan beweeg ik mijn hand een aantal keer van links naar rechts over mijn voorhoofd als teken dat ik aan het scannen ben maar niks ontvang. We noemen het gebaar thuis ‘De Knight Rider‘. Humor geeft lucht en een erkennen en accepteren van wat op dit moment even zo is. Er komt wel weer een ander moment.
En nu jij
Ik denk dat wij ontzettend veel van elkaars omweggetjes zouden kunnen leren. Daarom wil ik je een vraag stellen:
Herken jij dat je soms vastloopt in je denken en voelen? Dat het je simpelweg niet lukt om te starten met een cognitieve taak? En hebben jij en je naasten daar omweggetjes omheen gevonden? Laat het me weten. Als je helemaal naar beneden scrollt op deze pagina, kun je in de comments jouw tips achterlaten. Of mail me op sparks@verbeeldingskr8.nl. Ik ben heel benieuwd!
Ik hoop met jullie input een mooie lijst te kunnen samenstellen. Geïllustreerd natuurlijk. Dat beloof ik : -)

Sparks
Bronnen
(1) Timmer, M.H.M. (2019). Out of Balance. Neurocognitive mechanisms underlying depression in Parkinson’s disease. [THESIS]. Retrieved from https://books.ipskampprinting.nl/thesis/529302-Timmer/ (Open Access)
(2) Parent, M., & Parent, A. (2010). Substantia Nigra and Parkinson’s Disease: A Brief History of Their Long and Intimate Relationship. Canadian Journal of Neurological Sciences / Journal Canadien Des Sciences Neurologiques, 37(3), 313-319. https://doi.org/10.1017/S0317167100010209. Retrieved from http://www.biusante.parisdescartes.fr/chn/docpdf/parent_10_2017%20(3).pdf (Green Open Access)
(3) , et al (2017). What a neurologist should know about depression in Parkinson’s disease. (Closed Access, or see Chapter 2 of Monique’s Thesis at https://books.ipskampprinting.nl/thesis/529302-Timmer/ for the Open Access version)
(4) Goldman, J.G., et al (2018). Cognitive impairment in Parkinson’s disease: a report from a multidisciplinary symposium on unmet needs and future directions to maintain cognitive health. npj Parkinson’s Disease 4, Article number: 19. Retrieved from https://doi.org/10.1038/s41531-018-0055-3 (Open Access)
Over Monique Timmer

Monique Timmer (1982) studeerde medicijnen aan de Universiteit Utrecht. In 2008 startte ze haar neurologie opleiding bij het Radboud UMC in Nijmegen. In 2011 startte ze met een promotieonderzoek naar de neurocognitieve aspecten van de ziekte van Parkinson. Sinds oktober 2018 werkt ze als neuroloog bij het Radboud UMC en het Parkinson Centrum in Nijmegen.
mental freezing –ik voel het soms niet aankomen of ik herken het niet – ineens is het dan zo dus kan ik het niet aankondigen
raak soms even in paniek tot mijn eigen verbazing en verontrusting – na een aantal nachten goed slapen is het minder sterk = maar ik slaap vaak slecht / weinig en wordt daardoor kwetsbaar
nog een vraag is depressie bij parkinson wel een echte depressie en meer een symptomencluster van parkinson? en is het dan wel goed om nortriptiline te slikken?
Ha Willem, dank voor je reactie. Klopt dat mental freezing er ineens is. Toch is het mijn ervaring als je daarna bedenkt wat er gebeurde dat je er retrospectief wel degelijk omwegen omheen kunt vinden. Misschien vind je het leuk om eens op https://www.copiedstudie.nl te kijken.
Je vraag is een hele goede. Depressie kan gewoon bij Parkinson horen en in die zien inderdaad een symptomencluster zijn van parkinson. Of het dan goed is om nortriptiline te slikken kan ik je niet vertellen. Dat kun je het beste aan je neuroloog vragen? Groet, Marina